Materi Zat Campuran Homogen Larutan Asam dan Basa
SEKARANG kita belajar tentang zat campuran. Pada pelajaran sebelumnya, materi yang ada di alam dapat diklasifikasi berdasarkan komposisinya menjadi zat tunggal (murni) dan campuran. Zat tunggal terdiri atas unsur dan senyawa. Zat campuran terbagi atas heterogen dan homogen.
Zat yang heterogen punya dua jenis yakni koloid dan suspensi. Zat yang homogen berbentuk dalam larutan. Lebih jelasnya, mari kita fokus mempelajari zat campuran sebagaimana dikutip dari buku Ilmu Pengetahuan Alam Untuk SMP/MTs Kelas VII Semester 1 dengan penulis Wahono Widodo, Fida Rachmadiarti, dan Siti Nurul Hidayati.
Pengertian campuran
Campuran adalah suatu materi yang terdiri atas dua zat atau lebih yang masih punya sifat zat asalnya. Contoh beberapa campuran yang sering kita jumpai dalam kehidupan sehari-hari yaitu susu cokelat, air sungai, udara, batuan, garam beryodium, dan paduan logam.
Baca juga: Unsur dan Senyawa sebagai Materi Zat Tunggal
Kita sering menggunakan berbagai jenis campuran, semisal memasak dan membuat teh manis atau kopi. Campuran adalah suatu materi yang terdiri atas dua zat atau lebih yang masih punya sifat zat asalnya. Campuran dibedakan menjadi dua, yaitu campuran homogen dan campuran heterogen.
Campuran homogen
Campuran homogen banyak kita jumpai dalam kehidupan sehari-hari. Larutan gula, larutan garam, dan sirop merupakan contoh campuran homogen. Dalam larutan gula, apakah kita dapat membedakan zat-zat penyusunnya? Tentu saja tidak. Jadi, campuran homogen adalah campuran yang tidak dapat dibedakan zat-zat yang tercampur di dalamnya.
Baca juga: Klasifikasi Materi Berdasarkan Wujud: Padat, Cair, Gas
Larutan tersusun atas pelarut (solvent) dan zat terlarut (solute). Pelarut yang banyak digunakan ialah air. Senyawa lain yang dapat digunakan sebagai pelarut ialah senyawa organik yang dikenal juga sebagai pelarut organik, contohnya kloroform dan alkohol.
Dalam larutan, ukuran partikel zat terlarut sangat kecil dengan diameter kurang dari 1 nanometer (nm) sehingga partikel zat terlarut tidak dapat dilihat walaupun menggunakan mikroskop ultra. Oleh karena itu, larutan terlihat homogen (serbasama). Artinya zat yang terlarut dan pelarut dalam larutan tersebut tidak dapat dibedakan.
1. Larutan asam.
Contoh campuran homogen ialah larutan. Pada dasarnya, larutan yang dikenal dalam kehidupan sehari-hari dapat dikelompokkan menjadi larutan bersifat asam, basa, atau garam. Larutan seperti cuka, sirop, penghilang noda, sabun cuci, sabun mandi, soda kue, dan garam dapur merupakan contoh larutan asam, basa, atau garam yang banyak dijumpai setiap hari.
Baca juga: Mempelajari Hewan Avertebrata dan Vertebrata
Larutan asam dan basa dimanfaatkan secara luas untuk industri, pertanian, kesehatan, dan penelitian di laboratorium. Oleh karena itu, dalam memahami sifat-sifat asam dan basa merupakan hal yang sangat penting untuk memahami berbagai macam jenis larutan yang dijumpai dalam kehidupan sehari-hari.
Asam banyak ditemukan dalam buah-buahan dan sayuran. Contohnya, jeruk, lemon, dan tomat. Pada saat memasak di dapur, tentu kamu mengenal salah satu bahan penambah rasa makanan, yaitu cuka dapur yang mengandung asam asetat. Aki pada kendaraan bermotor mengandung asam sulfat.
Baca juga: Cara Klasifikasi Makhluk Hidup Menurut Carolus Linnaeus
Asam dalam lambung kita, yaitu asam klorida berfungsi membantu proses pencernaan bahan makanan. Masih banyak contoh senyawa asam lain yang dikenal dalam kehidupan sehari-hari. Kamu dapat menemukan larutan asam, baik dalam makanan, minuman, ataupun bahan pembersih di rumah.
Ciri atau tanda dari larutan asam.
a. Rasanya asam (tidak boleh dicoba kecuali dalam makanan).
b. Dapat menimbulkan korosi.
c. Mengubah kertas lakmus biru menjadi merah.
Selain banyak dimanfaatkan dalam kehidupan sehari-hari, larutan asam dapat menimbulkan dampak negatif bagi lingkungan, contohnya terjadihujan asam. Di beberapa wilayah tertentu, terjadi hujan asam yang menyebabkan kerusakan pada bangunan gedung dan patung-patung dalam kota.
Mengapa dapat terjadi hujan asam?
Bila terdapat kadar gas belerang dioksida (SO2) dan nitrogen oksida (NO) di atmosfer sangat tinggi, gas ini akan bereaksi dengan air di atmosfer dan membentuk asam sulfat, asam nitrat, dan senyawa asam lain. Ketika terjadi hujan, air yang dihasilkan bersifat lebih asam dari keadaan normal. Air hujan inilah yang dikenal dengan hujan asam.
Gas belerang dioksida dan gas nitrogen oksida dihasilkan dari pembakaran minyak bumi yang berasal dari buangan industri dan kendaraan bermotor. Selain merusak gedung dan patung-patung, hujan asam tersebut dapat merusak tumbuh-tumbuhan dan dapat menyebabkan kematian pada makhluk hidup yang ada di sungai apabila hujan asam tersebut masuk ke sungai.
2. Larutan basa.
Basa merupakan larutan yang banyak dijumpai dalam kehidupan sehari-hari. Contoh benda yang mengandung basa ialah sabun mandi, sabun cuci, sampo, pasta gigi, obat mag, dan pupuk. Dalam penggunaan sehari-hari, umumnya basa dicampur dengan zat lain.
Sifat-sifat larutan basa.
a. Punyai rasa agak pahit (tidak boleh dicoba).
b. Terasa licin di kulit.
c. Mengubah kertas lakmus merah menjadi biru.
Dalam kehidupan sehari-hari, larutan asam sering direaksikan dengan larutan basa untuk menghasilkan senyawa netral atau dikenal dengan reaksi netralisasi. Pada reaksi netralisasi ini akan dihasilkan garam dan air.
Contoh penerapan reaksi netralisasi dalam kehidupan sehari-hari ialah pengobatan bagi penderita sakit mag. Sakit mag punya kondisi kadar asam lambung yang tinggi. Karenanya, obat mag ialah senyawa yang bersifat basa (kandungannya magnesium hidroksida atau aluminium hidroksida).
Contoh lain yaitu pengobatan akibat sengatan serangga, perlindungan terhadap kerusakan gigi, dan pengolahan tanah pertanian.
Larutan asam dan larutan basa memiliki sifat-sifat yang khas. Salah satu cara untuk membedakan asam atau basa dapat menggunakan indikator. Suatu indikator asam-basa ialah senyawa yang dapat menunjukkan perubahan warna apabila bereaksi dengan asam atau basa. Indikator asam-basa dapat dibedakan menjadi indikator alami dan indikator buatan.
a. Indikator alami.
Berbagai jenis tumbuhan dapat digunakan sebagai indikator alami. Tumbuhan yang termasuk indikator alami akan menunjukkan perubahan warna pada larutan asam ataupun basa. Beberapa contoh tumbuhan yang dapat digunakan sebagai indikator alami ialah kunyit, bunga mawar, kubis merah, kubis ungu, dan bunga kembang sepatu.
Ekstrak kunyit akan memberikan warna kuning cerah pada larutan asam dan dalam larutan basa akan memberikan warna jingga. Kubis (kol) merah mengandung suatu zat indikator,yaitu antosianin. Zat ini berwarna merah pada asam, berwarna hijau pada basa lemah, dan berwarna kuning pada basa kuat.
Ekstrak bunga kembang sepatu akan memberikan warna merah cerah jika diteteskan dalam larutan asam. Jika diteteskan dalam larutan basa akan dihasilkan warna hijau.
b. Indikator buatan.
Salah satu jenis indikator buatan yang bukan dalam bentuk larutan cair ialah kertas lakmus. Ada dua jenis kertas lakmus, yaitu lakmus biru dan lakmus merah. Warna kertas lakmus biru akan menjadi merah dalam larutan asam. Warna kertas lakmus merah akan menjadi biru dalam larutan basa.
3. Larutan garam.
Jenis senyawa garam yang paling dikenal ialah garam dapur atau nama senyawa kimianya natrium klorida (NaCl). Garam ini banyak digunakan dalam pengolahan makanan.
Bagaimana senyawa garam dapat terbentuk? Salah satu reaksi yang dapat membentuk garam adalah reaksi asam dan basa atau reaksi netralisasi. Pada reaksi netralisasi tersebut akan dihasilkan garam dan air.
Asam + Basa ---> Garam + Air
Garam secara luas digunakan dalam kehidupan sehari-hari, antara lain untuk industri pupuk, obat-obatan, pengolahan makanan, dan bahan pengawet. Contoh reaksi asam dan basa yang membentuk berbagai jenis garam.
HCl + NaOH ---> NaCl + H2O
Asam klorida + Natrium hidroksida ---> Garam NaCl + air
Campuran heterogen
Berbeda dengan larutan gula, pada campuran pasir dan air, kita masih dapat membedakan antara pasir dan air. Campuran pasir dan air merupakan salah satu contoh dari campuran heterogen.
Campuran heterogen terjadi karena zat tidak dapat bercampur satu dengan yang lain secara sempurna sehingga dapat dikenali zat penyusunnya. Dengan demikian, pada campuran heterogen, seluruh bagiannya tidak memiliki komposisi yang sama (tidak serbasama).
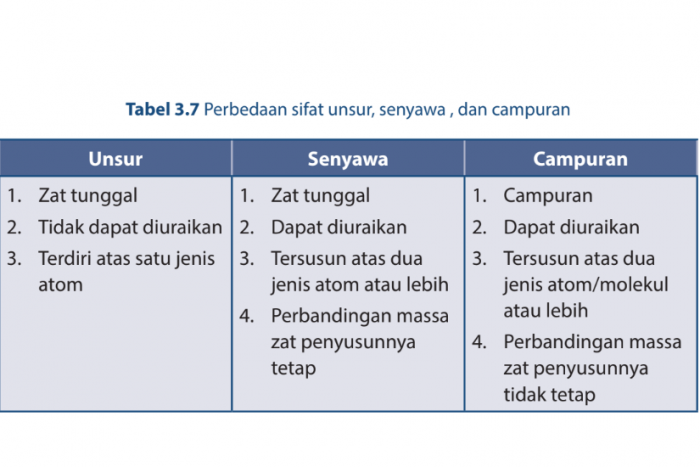
Sekarang apakah kamu sudah memahami dengan jelas mengenai perbedaan unsur, senyawa, dan campuran? Berikut perbedaan sifat unsur, senyawa, dan campuran.
Sifat unsur
1. Zat tunggal.
2. Tidak dapat diuraikan.
3. Terdiri atas satu jenis atom.
Sifat senyawa
1. Zat tunggal.
2. Dapat diuraikan.
3. Tersusun atas dua jenis atom atau lebih.
4. Perbandingan massa zat penyusunnya tetap.
Sifat campuran
1. Campuran.
2. Dapat diuraikan.
3. Tersusun atas dua jenis atom/molekul atau lebih.
4. Perbandingan massa zat penyusunnya tidak tetap.
Itulah pembahasan tentang zat campuran yang terdiri dari zat heterogen dan homogen. Jangan malas belajar dan membaca ya. (Z-2)
Terkini Lainnya
Pengertian campuran
Campuran homogen
1. Larutan asam.
2. Larutan basa.
3. Larutan garam.
Campuran heterogen
Tim Olimpiade Fisika Indonesia Borong Penghargaan di Asian Physics Olympiad di Malaysia
Dunia Paralel: Penjelasan Teori dan Penemuan Para Ilmuwan
Hebat! Siswa Ini Raih Penghargaan di Singapore and Asian Schools Math Olympiad
Prof Dadang Juandi: Tingkatkan Peran Meta-Analisis dalam Evaluasi dan Pengembangan Pembelajaran Matematika
Guru Besar UPI: Penguatan Higher Order Thinking Skill dapat Dilakukan Melalui Pembelajaran Fisika pada Pendidikan Vokasional
Cara Menghitung Rumus Percepatan dan Contoh Soalnya untuk Pelajaran Fisika
LTLS Tebar Dividen Rp35 per Saham, Cair 13 Juni
Proses Penyelidikan Ilmiah IPA dan Hasil Kumpulan Pengetahuannya
Kopi Tanpa Kafein: Apa yang Harus Diketahui dan Dilakukan?
Honeywell Dukung Indonesia Capai Net Zero Emission dengan Teknologi CCUS
Saatnya Pengusaha Lokal Investasi di Bidang Kimia Konstruksi
Kurangi Penggunaan Pupuk Kimia, Kementan Perkenalkan Inovasi Teknik Biosaka
Umur di Tangan Tuhan, Bantuan Hidup Dasar Mesti Dilakukan
Sengkarut-marut Tata Kelola Pertanahan di IKN
Panggung Belakang Kebijakan Tapera
Pancasila, Perempuan, dan Planet
Eskalasi Harga Pangan Tengah Tahun
Iuran Tapera ibarat Masyarakat Berdiri di Air Sebatas Dagu
Polresta Malang Kota dan Kick Andy Foundation Serahkan 37 Kaki Palsu
Turnamen Golf Daikin Jadi Ajang Himpun Dukungan Pencegahan Anak Stunting
Kolaborasi RS Siloam, Telkomsel, dan BenihBaik Gelar Medical Check Up Gratis untuk Veteran
Ulang Tahun, D'Cost Donasi ke 17 Panti Asuhan Melalui BenihBaik.com
Informasi
Rubrikasi
Opini
Ekonomi
Humaniora
Olahraga
Weekend
Video
Sitemap