Perubahan Materi secara Fisika dan Kimia serta Ciri-Cirinya
BENDA-BENDA yang kita kenal dalam kehidupan sehari-hari sering kali mengalami perubahan. Perubahan tersebut ada yang bersifat langsung dapat diamati. Ada juga yang memerlukan waktu lama untuk pengamatannya. Perubahan benda-benda tersebut dikenal dengan perubahan materi mencakup sifat fisika dan kimia.
Contoh perubahan materi yang berlangsung cepat ialah pembakaran kertas. Contoh perubahan materi yang memerlukan waktu yang relatif lama ialah proses berkaratnya besi.
Sebelum lebih jauh membahas tentang perubahan materi, kamu perlu mengetahui tentang sifat-sifat zat terlebih dahulu. Sifat-sifat benda sangat penting diketahui untuk membedakan perubahan-perubahan yang terjadi pada benda tersebut.
Baca juga: Lima Cara Memisahkan Campuran: Penyaringan, Sentrifugasi, Sublimasi, Kromatografi, Distilasi
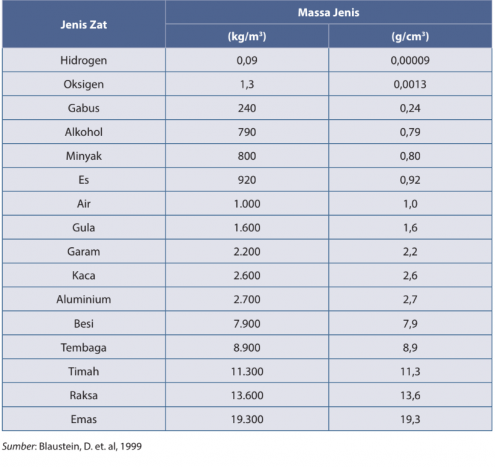
Sifat-sifat benda secara garis besar dibedakan menjadi dua, yaitu sifat fisika dan sifat kimia. Sifat fisika adalah sifat yang berkaitan dengan keadaan fisik suatu zat. Sifat fisika termasuk bentuk, warna, bau, kekerasan, titik didih, titik beku, titik leleh, daya hantar, ukuran partikel, dan massa jenis (densitas).
Sifat kimia merupakan sifat zat yang berhubungan dengan mudah atau sukarnya zat tersebut untuk bereaksi secara kimia. Demikian dikutip dari buku Ilmu Pengetahuan Alam Untuk SMP/MTs Kelas VII Semester 1 dengan penulis Wahono Widodo, Fida Rachmadiarti, dan Siti Nurul Hidayati.
Baca juga: Materi Zat Campuran Homogen Larutan Asam dan Basa
Zat yang sama memiliki massa jenis yang sama, tidak peduli jumlah zat itu. Contoh, massa jenis air 1 g/cm3. Sesendok air, sepanci air, ataupun sekolam air, massa jenisnya tetap 1 g/cm3. Jika kamu menemukan zat cair yang massa jenisnya 1 g/cm3, kamu dapat memperkirakan bahwa kemungkinan besar zat tersebut ialah air. Jadi, selain wujud zat dan partikel penyusunnya, massa jenis merupakan salah satu penanda zat itu.
Contoh masalah
Edo menemukan sebongkah logam. Ia penasaran jenis logam yang ditemukannya. Ia berpikir jangan-jangan emas. Edo menimbang logam itu. Ternyata massanya 312,0 gram. Dengan gelas ukur, Edo mengukur volumenya. Kemungkinan besar, logam apa yang ditemukan Edo?
Langkah-langkah pemecahan masalah
Diketahui massa logam = 312,0 gram.
Baca juga: Unsur dan Senyawa sebagai Materi Zat Tunggal
Volume logam = volume air dan logam – volume air = 100 mL – 60 mL = 40 mL = 40 cm3.
Apa masalahnya?
Menentukan jenis logam
Bagaimana strateginya?
Gunakan prinsip bahwa massa jenis merupakan penciri zat.
Bagaimana penerapannya?
ρ = m/v
= 312 gram/40 cm3.
= 7,8 g/cm3.
Apa kesimpulannya?
Dengan membandingkan hasil pengukuran massa jenis dengan nilai pada massa jenis zat, nilai massa jenis yang paling dekat yaitu massa jenis besi (7,9 g/cm3). Jadi, kemungkinan besar logam yang ditemukan Edo ialah besi.
Perubahan fisika
Hasil pengamatanmu di atas menunjukkan bahwa perubahan materi ada yang tidak menghasilkan zat baru. Ada pula yang menghasilkan zat yang baru. Perubahan zat yang tidak disertai dengan terbentuknya zat baru disebut perubahan fisika.
Baca juga: Klasifikasi Materi Berdasarkan Wujud: Padat, Cair, Gas
Komposisi materi tersebut juga tidak akan berubah, misalnya es yang mencair. Baik dalam bentuk padat maupun dalam bentuk cair keduanya tetaplah air, yaitu H2O. Contoh perubahan fisika antara lain menguap, mengembun, mencair, membeku, menyublim, melarut, serta perubahan bentuk lain.
Perubahan kimia
Perhatikan kayu yang dibakar. Apakah kayu sebelum dan setelah dibakar akan menghasilkan zat yang sama? Kayu sebelum dibakar mengandung serat selulosa, tetapi setelah dibakar berubah menjadi arang atau karbon. Dengan demikian, pada proses pembakaran kayu diperoleh zat baru yang memiliki sifat berbeda dengan zat sebelumnya.
Proses pembakaran kayu yang mengakibatkan terbentuknya zat baru merupakan salah satu contoh perubahan kimia. Contoh lain perubahan kimia yang sering terjadi di alam ialah proses perkaratan besi. Besi sebelum berkarat merupakan unsur Fe, tetapi besi setelah berkarat berubah menjadi senyawa Fe2O3nH2O. Dengan demikian, kita dapat mendefinisikan bahwa perubahan kimia adalah perubahan zat yang menghasilkan zat baru dengan sifat kimia yang berbeda dengan zat asalnya.
Zat baru yang terbentuk dalam perubahan kimia disebabkan ada perubahan komposisi materi. Perubahan tersebut dapat berupa penggabungan sejumlah zat atau peruraian suatu zat. Berlangsungnya perubahan kimia dapat diketahui dengan ciri-ciri sebagai berikut.
1. Terbentuk zat baru.
2. Terbentuk gas.
3. Terbentuk endapan.
4. Terjadi perubahan warna.
5. Terjadi perubahan suhu.
Salah satu ciri perubahan kimia ialah terbentuk zat baru. Selain terbentuk zat baru, ciri perubahan kimia lainnya adalah terbentuknya gas dan endapan.
Bagaimanakah proses terbentuknya gas dan endapan tersebut? Simaklah penjelasan berikut dengan seksama.
a. Pembentukan gas.
Reaksi kimia bersifat unik. Beberapa reaksi kimia tertentu dapat membentuk gas. Contoh reaksi kimia yang membentuk gas ialah reaksi logam magnesium (Mg) dengan asam klorida (HCl).
Reaksi tersebut dapat ditulis sebagai berikut.
Magnesium + Asam klorida ---> Magnesium klorida + gas hidrogen
Mg + 2HCl ---> MgCl2 + H2
Gas yang terbentuk dapat kamu lihat dalam wujud gelembung-gelembung kecil. Gas tersebut ialah gas hidrogen. Contoh reaksi pembentukan gas yang lain ialah reaksi elektrolisis air (H2O) menjadi gas hidrogen (H2) dan oksigen (O2).
b. Pembentukan endapan.
Reaksi pengendapan ialah reaksi yang menghasilkan suatu senyawa yang berbentuk padatan. Padatan tersebut tidak larut (tidak bercampur secara homogen) dengan cairan di sekitarnya sehingga disebut endapan.
Salah satu contoh reaksi yang dapat membentuk endapan ialah reaksi antara barium klorida (BaCl2) dengan natrium sulfat (Na2SO4) menghasilkan endapan barium sulfat berwarna putih. Reaksi tersebut berlangsung sebagai
berikut.
Barium klorida + Natrium sulfat ---> Endapan putih Barium sulfat + Natrium klorida
Contoh reaksi pembentukan endapan yang lain ialah reaksi antara timbal nitrat (Pb(NO3)2) dengan natrium iodida (NaI) akan menghasilkan endapan timbal iodida yang berwarna kuning.
c. Perubahan warna.
Mengapa suatu reaski kimia dapat menghasilkan warna berbeda? Ketika suatu reaksi kimia berlangsung, akan terjadi perubahan komposisi dan terbentuk zat baru yang mungkin memiliki warna berbeda.
Contoh reaksi kimia yang memberikan warna yang khas ialah reaksi antara tembaga sulfat (CuSO4) dengan air (H2O). Warna tembaga sufat ialah putih. Bila ditambahkan air, warnanya berubah menjadi biru. Warna biru tersebut ialah warna senyawa baru yang terbentuk, yaitu CuSO4.5H2O.
d. Perubahan suhu.
Reaksi kimia disertai perubahan energi. Salah satu bentuk energi yang sering menyertai reaksi kimia ialah energi panas. Dengan demikian, perubahan kimia akan ditandai dengan perubahan energi panas atau aliran kalor dari atau ke lingkungan. Akibatnya, suhu hasil reaksi dapat menjadi lebih tinggi atau dapat menjadi lebih rendah daripada suhu pereaksinya.
Dari penjelasan tentang perubahan fisika dan perubahan kimia di atas, apakah kamu sudah memahami perbedaan antara perubahan fisika dengan perubahan kimia? Agar lebih paham berikut perbedaan perubahan fisika dengan perubahan kimia.
Perubahan fisika.
1. Tidak terbentuk zat baru.
2. Komposisi materi tidak berubah.
Perubahan kimia.
1. Terbentuk zat baru.
2. Komposisi materi sebelum dan sesudah reaksi mengalami perubahan atau perbedaan.
Contoh-contoh perubahan materi yang terjadi di alam.
Perubahan fisika.
1. Beras diubah menjadi tepung beras.
2. Kayu diubah menjadi kursi.
3. Gula dilarutkan dalam air.
4. Bola lampu listrik menyala.
5. Air berubah menjadi es.
Perubahan kimia.
1. Singkong menjadi tapai.
2. Pembakaran kayu.
3. Makanan basi.
4. Susu diubah menjadi keju.
5. Perkaratan besi.
Rangkuman
1. Materi berdasarkan wujudnya dikelompokkan menjadi zat padat, cair, dan gas.
2. Berdasarkan susunannya, materi yang ada di alam diklasifikasikan menjadi zat tunggal/murni (unsur, senyawa), dan campuran.
3. Unsur adalah zat tunggal/murni yang tidak dapat diuraikan menjadi zat-zat lain yang lebih sederhana dengan cara kimia.
4. Senyawa adalah zat tunggal/murni yang dapat diuraikan secara kimia menjadi dua zat atau lebih.
5. Campuran adalah suatu materi yang terdiri atas dua zat atau lebih dan masih punya sifat zat asalnya dengan tidak punya komposisi yang tetap.
6. Larutan adalah campuran yang homogen, tersusun atas zat terlarut dan pelarut.
7. Prinsip pemisahan campuran didasarkan pada perbedaan sifat-sifat fisis zat penyusunnya, seperti wujud zat, ukuran partikel, titik leleh, titik didih, sifat magnetik, dan kelarutan.
8. Beberapa metode pemisahan campuran yang sering digunakan antara lain penyaringan (filtrasi), sentrifugasi, sublimasi, kromatografi, dan destilasi.
9. Perubahan fisika adalah perubahan zat yang tidak disertai dengan terbentuknya zat baru.
10. Perubahan fisika meliputi menguap, mengembun, mencair, membeku, menyublim, melarut, serta perubahan bentuk.
11. Perubahan kimia adalah perubahan zat yang dapat menghasilkan zat baru dengan sifat kimia yang berbeda dengan zat asalnya.
12. Berlangsungnya perubahan kimia dapat diketahui dengan ciri-ciri sebagai berikut.
• Terbentuk zat baru.
• Terbentuk gas.
• Terbentuk endapan.
• Terjadi perubahan warna.
• Terjadi perubahan suhu. (Z-2)
Terkini Lainnya
Contoh masalah
Perubahan fisika
Perubahan kimia
a. Pembentukan gas.
b. Pembentukan endapan.
c. Perubahan warna.
d. Perubahan suhu.
Rangkuman
Tim Olimpiade Fisika Indonesia Borong Penghargaan di Asian Physics Olympiad di Malaysia
Dunia Paralel: Penjelasan Teori dan Penemuan Para Ilmuwan
Hebat! Siswa Ini Raih Penghargaan di Singapore and Asian Schools Math Olympiad
Prof Dadang Juandi: Tingkatkan Peran Meta-Analisis dalam Evaluasi dan Pengembangan Pembelajaran Matematika
Guru Besar UPI: Penguatan Higher Order Thinking Skill dapat Dilakukan Melalui Pembelajaran Fisika pada Pendidikan Vokasional
Cara Menghitung Rumus Percepatan dan Contoh Soalnya untuk Pelajaran Fisika
LTLS Tebar Dividen Rp35 per Saham, Cair 13 Juni
Proses Penyelidikan Ilmiah IPA dan Hasil Kumpulan Pengetahuannya
Kopi Tanpa Kafein: Apa yang Harus Diketahui dan Dilakukan?
Honeywell Dukung Indonesia Capai Net Zero Emission dengan Teknologi CCUS
Saatnya Pengusaha Lokal Investasi di Bidang Kimia Konstruksi
Kurangi Penggunaan Pupuk Kimia, Kementan Perkenalkan Inovasi Teknik Biosaka
Umur di Tangan Tuhan, Bantuan Hidup Dasar Mesti Dilakukan
Sengkarut-marut Tata Kelola Pertanahan di IKN
Panggung Belakang Kebijakan Tapera
Pancasila, Perempuan, dan Planet
Eskalasi Harga Pangan Tengah Tahun
Iuran Tapera ibarat Masyarakat Berdiri di Air Sebatas Dagu
Polresta Malang Kota dan Kick Andy Foundation Serahkan 37 Kaki Palsu
Turnamen Golf Daikin Jadi Ajang Himpun Dukungan Pencegahan Anak Stunting
Kolaborasi RS Siloam, Telkomsel, dan BenihBaik Gelar Medical Check Up Gratis untuk Veteran
Ulang Tahun, D'Cost Donasi ke 17 Panti Asuhan Melalui BenihBaik.com
Informasi
Rubrikasi
Opini
Ekonomi
Humaniora
Olahraga
Weekend
Video
Sitemap